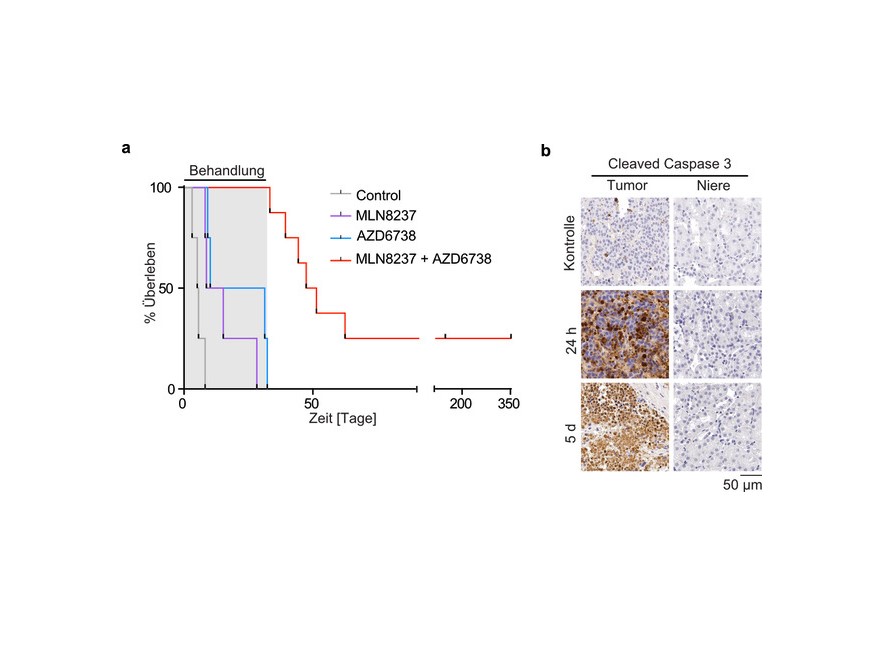
Überlebenskurve des TH-MYCN-Mausmodells bei Langzeitbehandlung mit Aurora-A-Inhibitor (lila), ATR-Inhibitor (blau) oder der Kombination aus beiden Wirkstoffen (rot). Deutlich ist erkennbar, dass die Kombinationstherapie die Überlebenszeit verlängert. (Bild: Gabriele Büchel / Universität Würzburg)
Mit zwei marktverfügbaren Hemmstoffen lässt sich bei der kindlichen Tumorerkrankung Neuroblastom der Zellzyklus der Krebszellen an einer Schlüsselstelle so stören, dass die Tumorzellen sterben.
Neuroblastome sind bösartige solide Tumoren, die vor allem im frühen Kindesalter auftreten. Sie entstehen aus entarteten unreifen Zellen des sympathischen Nervensystems.
Ein Anhaltspunkt, mit dem sich die Bösartigkeit des Tumors abschätzen lässt, ist das MYCN-Onkogen. Hochrisikopatienten des Neuroblastoms haben oft eine Amplifikation von MYCN, also sehr hohe Mengen dieses Proteins, was das unkontrollierte Tumorwachstum antreibt. Im Umkehrschluss könnte die Hemmung von MYCN oder seiner Funktion eine aussichtsreiche Therapiechance sein.
Einen wichtigen Schritt auf diesem Weg leistete eine kürzlich in der Zeitschrift Nature Cancer veröffentlichte, internationale Forschungsarbeit unter Leitung von Wissenschaftlerinnen der Julius-Maximilians-Universität Würzburg (JMU).
Neues über die Rolle von MYCN im Zellzyklus
Ko-Letztautorin der Publikation ist Dr. Gabriele Büchel vom Lehrstuhl für Biochemie und Molekularbiologie am Biozentrum der JMU. Die Arbeitsgruppenleiterin erläutert: „Bislang wusste man, dass MYCN die Funktion der RNA-Polymerase kontrolliert. Diese liest im Zellkern die DNA ab und stellt daraus die mRNA her. Durch unsere Forschungsarbeit konnten wir zeigen, dass MYCN außerdem eine spezifische Rolle während der S-Phase des Zellzyklus spielt, in der die DNA auch verdoppelt wird.“
In dieser Phase finden also zwei Prozesse gleichzeitig statt: das Ablesen und die Replikation der DNA. Bildlich gesprochen sind laut Gabriele Büchel „zwei Züge auf demselben Gleis unterwegs“.
Ziel: Transkriptions-Replikations-Konflikte fördern
Zusammen mit der Doktorandin Isabelle Roeschert fand sie heraus, dass MYCN Kollisionen beider Züge – sogenannte Transkriptions-Replikations-Konflikte – verhindert.
Für diese Signalwirkung sind die zwei Enzyme Aurora-A und ATR notwendig, die man beide mit vorhandenen Pharmaka hemmen kann. Auf diese Weise können gezielt „Zugkollisionen“ herbeigeführt werden, um die Tumorzelle zu schädigen. Oder medizinisch ausgedrückt: Die Kombination beider Wirkstoffe führt zu DNA-Schäden und Zelltod – und zwar hochspezifisch in Tumoren, während andere Gewebe unbeeinflusst bleiben.
„In Mausmodellen des Neuroblastoms konnten wir durch diese Strategie eine Regression des Tumorwachstums erreichen. Ein Teil der Versuchstiere konnte mit dieser Strategie geheilt werden“, verdeutlicht Gabriele Büchel den Effekt dieser „Therapie“.
Klinische Studien schon am Horizont
Nach ihren Angaben könnten auch Patientinnen und Patienten zeitnah von den gewonnenen Erkenntnissen profitieren. „Die von uns eingesetzten Substanzen sind alle bereits auf dem Markt. Aurora-A- und ATR-Inhibitoren sowie die von uns eingesetzten Kombinationen werden zurzeit in einer Reihe von praxisnahen Modellen geprüft. Wenn sie da erfolgreich sind, könnten bald klinische Studien beginnen“, kündigt Büchel an.
Neben der JMU-Arbeitsgruppe waren Forschungsteams der Charité in Berlin, der Universitäten Göttingen und Zürich sowie des Institute of Cancer Research in London an der Studie beteiligt. Gefördert wurde sie von der Deutschen Krebshilfe und vom Europäischen Forschungsrat.
Publikation
Combined inhibition of Aurora-A and ATR kinases results in regression of MYCN-amplified neuroblastoma. Nature Cancer, 11. Februar 2021, DOI: 10.1038/s43018-020-00171-8
Kontakt
Biozentrum, Universität Würzburg
Frau Dr. Gabriele Büchel
T +49 931 31-84946, gabriele.buechel@uni-wuerzburg.de
Beitrag von Helmuth Ziegler,Universität Würzburg