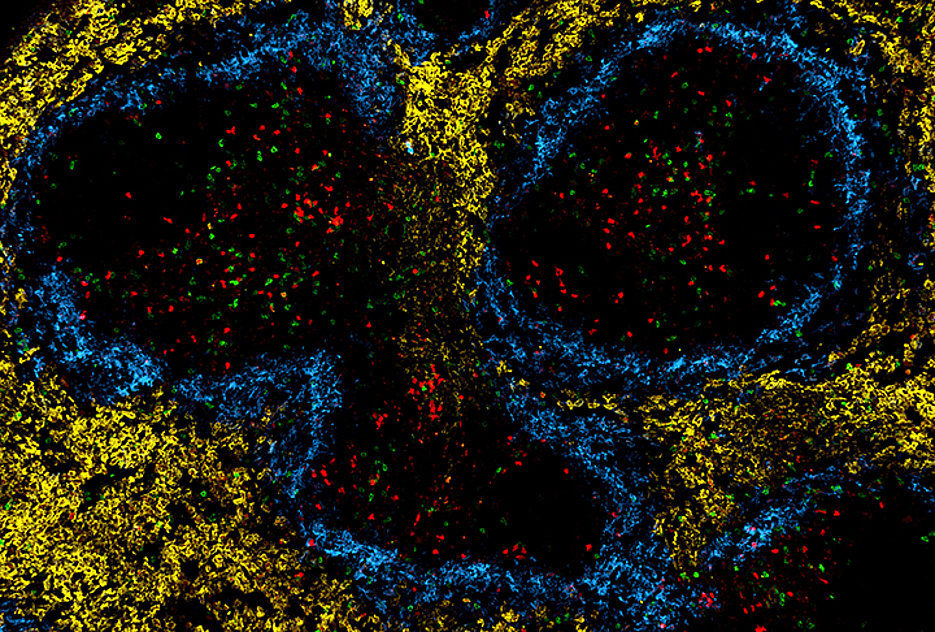
Gesunde (rot) und erschöpfte (grün) T-Zellen in der Milz einer chronisch infizierten Maus. (Bild: Ana Maria Mansilla / Institut für Systemimmunologie, Universität Würzburg)
Beim Kampf des Immunsystems gegen Krebs und chronische Infektionen lässt oft die Schlagkraft der T-Zellen nach. Das Team des Immunologen Martin Väth hat eine mögliche Erklärung dafür gefunden.
Im Immunsystem kommt es bei chronischen Infektionen und bei der Abwehr von Tumoren oft zum Phänomen der T-Zell-Erschöpfung: Dabei verlieren die T-Lymphozyten schrittweise ihre Funktion, und das beeinträchtigt die Immunreaktion gegen Krebs und Infektionen. Die molekularen Mechanismen, die diesen Funktionsverlust steuern, sind noch nicht vollständig entschlüsselt.
Jetzt steht fest, dass der Erschöpfungsprozess maßgeblich von den „Kraftwerken“ der T-Zellen, den Mitochondrien, beeinflusst wird.
Fällt die mitochondriale Zellatmung aus, setzt das eine Folge von Reaktionen in Gang, an deren Ende die T-Zellen genetisch und metabolisch umprogrammiert werden – und das treibt ihre Erschöpfung voran. Doch dem „Burnout“ der T-Zellen lässt sich entgegenwirken: Eine pharmakologische oder genetische Optimierung des zellulären Stoffwechsels erhöht die Langlebigkeit und die Funktionalität von T-Zellen. Das gelingt zum Beispiel durch die Überexpression eines mitochondriellen Transporters, der für die Produktion des energieliefernden Moleküls Adenosin-Triphosphat notwendig ist.
Das berichtet ein Team um Dr. Martin Väth vom Institut für Systemimmunologie der Julius-Maximilians-Universität (JMU) Würzburg im Journal Nature Communications. „Wir hoffen, dass sich mit Hilfe unserer Ergebnisse Immuntherapien gegen Krebs weiter verbessern lassen“, sagt der Wissenschaftler.
Mögliche Verbesserung der CAR-T-Zelltherapie
Ein Beispiel: Mit CAR-T-Zellen können bei Leukämie- und Lymphom-Erkrankungen beachtliche Erfolge erzielt werden. Es handelt sich dabei um T-Zellen, die im Labor für den Kampf gegen die jeweilige Krebsform fit gemacht wurden. Doch gegen solide Tumoren haben CAR-T-Zellen oft nur begrenzten Erfolg, weil auch sie bei dieser Arbeit „erschöpfen“.
„Unsere Experimente zeigen außerdem, dass ein gesteigerter mitochondrieller Stoffwechsel auch die Langlebigkeit und Funktionalität von Virus-spezifischen T-Zellen bei chronischen Infektionen steigert“, so der JMU-Forscher. Womöglich hat sein Team hier auch eine Stellschraube gefunden, über die sich T-Zell-basierte Immuntherapien gegen Krebs verbessern lassen.
Die Experimente im Detail
„Bisher ging man davon aus, dass die beobachteten Veränderungen im (Energie-)Stoffwechsel der Mitochondrien eine Folge der T-Zell-Erschöpfung sind“, so Väth. Um einen direkten und kausalen Zusammenhang zwischen einem veränderten mitochondriellen Stoffwechsel und dem Funktionsverlust von erschöpften T-Zellen zu zeigen, entwickelte seine Forschungsgruppe ein neues genetisches Modell. Es schaltet den mitochondriellen Phosphat-Transporter (SLC25A3) aus und legt die Zellatmung in den Mitochondrien lahm.
Als Folge sind die T-Zellen gezwungen, auf alternative Stoffwechselwege auszuweichen, insbesondere auf die aerobe Glykolyse, um ihren Bedarf an chemischer Energie in Form von Adenosin-Triphosphat zu decken. Diese metabolische Anpassung führt dann zur vermehrten Bildung von Sauerstoffradikalen in den T-Zellen.
Die erhöhten Sauerstoffradikal-Level verhindern den Abbau des wichtigen Transkriptionsfaktors hypoxia-inducible factor 1 alpha (HIF-1-alpha) auf Proteinebene. Der Faktor reichert sich dadurch im Zellkern an. Das bewirkt eine genetische und metabolische Umprogrammierung der T-Zellen und beschleunigt deren Erschöpfung.
„Diese HIF-1-alpha-abhängige Kontrolle der T-Zell-Erschöpfung war bisher unbekannt. Sie stellt einen bedeutenden Regelkreis zwischen der Zellatmung und der Funktion von T-Zellen dar, den wir als ‚metabolischen Kontrollpunkt‘ der T-Zell-Erschöpfung bezeichnen können“, erklärt Väth.
Gewebe als Umfeld der T-Zellen berücksichtigen
Als nächstes will sein Team erforschen, wie die mitochondriale Zellatmung die epigenetische Programmierung von T-Zellen beeinflusst, beispielsweise durch posttranslationale Modifikationen von Histonen. Dabei sollen auch die Auswirkungen berücksichtigt werden, die das Gewebe als direktes Umfeld auf die T-Zellen hat.
Laut Martin Väth ist das besonders wichtig, weil sich Nährstoffgehalt, Sauerstoffsättigung und andere metabolische „Stressfaktoren“ in Tumoren teilweise erheblich von gesundem Gewebe unterscheiden und weil T-Zellen aktiv auf diese Umgebung reagieren müssen. Neue technische Entwicklungen, wie räumliche Transkriptom- und Metabolom-Analysen, bieten erstmals die Möglichkeit, diese Fragen systematisch und hochauflösend im Gewebeumfeld zu untersuchen.
Publikation
Mitochondrial dysfunction promotes the transition of precursor to terminally exhausted T cells through HIF-1α-mediated glycolytic reprogramming. Nature Communications 14, 6858 (2023), DOI 10.1038/s41467-023-42634-3.
Open Access: https://www.nature.com/articles/s41467-023-42634-3
Kooperationspartner
Der Großteil der beschriebenen Arbeiten ist in Martin Väths Labor gelaufen. Die metabolischen Analysen wurden bei Professor Bart Ghesquière an der Katholischen Universität Leuven (Belgien) durchgeführt. Die Einzelzell-Analysen erfolgten in Kooperation mit dem Single-Cell Center des Würzburger Helmholtz-Instituts für RNA-basierte Infektionsforschung (HIRI).
Förderer
Finanziell unterstützt wurde die Studie von der Deutschen Forschungsgemeinschaft (DFG) im Rahmen des Transregio 338 „Lymphocyte engineering for therapeutic synthethic immunity“ (Würzburg-München) und des Sonderforschungsbereichs 1525 „Cardioimmune-Interfaces“ (Würzburg).
Kontakt
Dr. Martin Väth, Leiter einer Nachwuchsgruppe an der Max-Planck Forschungsgruppe für Systemimmunologie, Universität Würzburg, T +49 931 31-82491, martin.vaeth1@uni-wuerzburg.de